近日,华中科技大学张胜民教授团队在综合类顶级期刊《国家科学评论》(National Science Review)发表题为“3D micropattern force triggers YAP nuclear entry by transport across nuclear pores and modulates stem cells paracrine”的研究论文,首次阐明了3D微图案触发人骨髓间充质干细胞的力学信号转导及其对干细胞旁分泌功能和组织再生的影响。《国家科学评论》同期配发了美国三院院士Antonios G. Mikos教授对该论文的亮点述评,认为该工作将为新一代细胞/基因活性生物材料的创新设计和表面微纳工程提供重要启示。

图1. 《国家科学评论》(National Science Review)发表张胜民教授团队原创研究
生物材料表面二维微图案已被证明可调节干细胞行为。然而干细胞在体内处于复杂的三维微环境中,对二维微图案的研究并不能反映天然真实微环境中干细胞周围的关键力学特征。3D微图案如何触发干细胞力学信号转导进而调节干细胞功能和组织再生仍不清楚,尤其缺乏体内实验证据。因此,研究干细胞在3D微图案中的力学信号转导具有重要意义,将为组织诱导型生物材料的表面形貌设计提供重要指导。
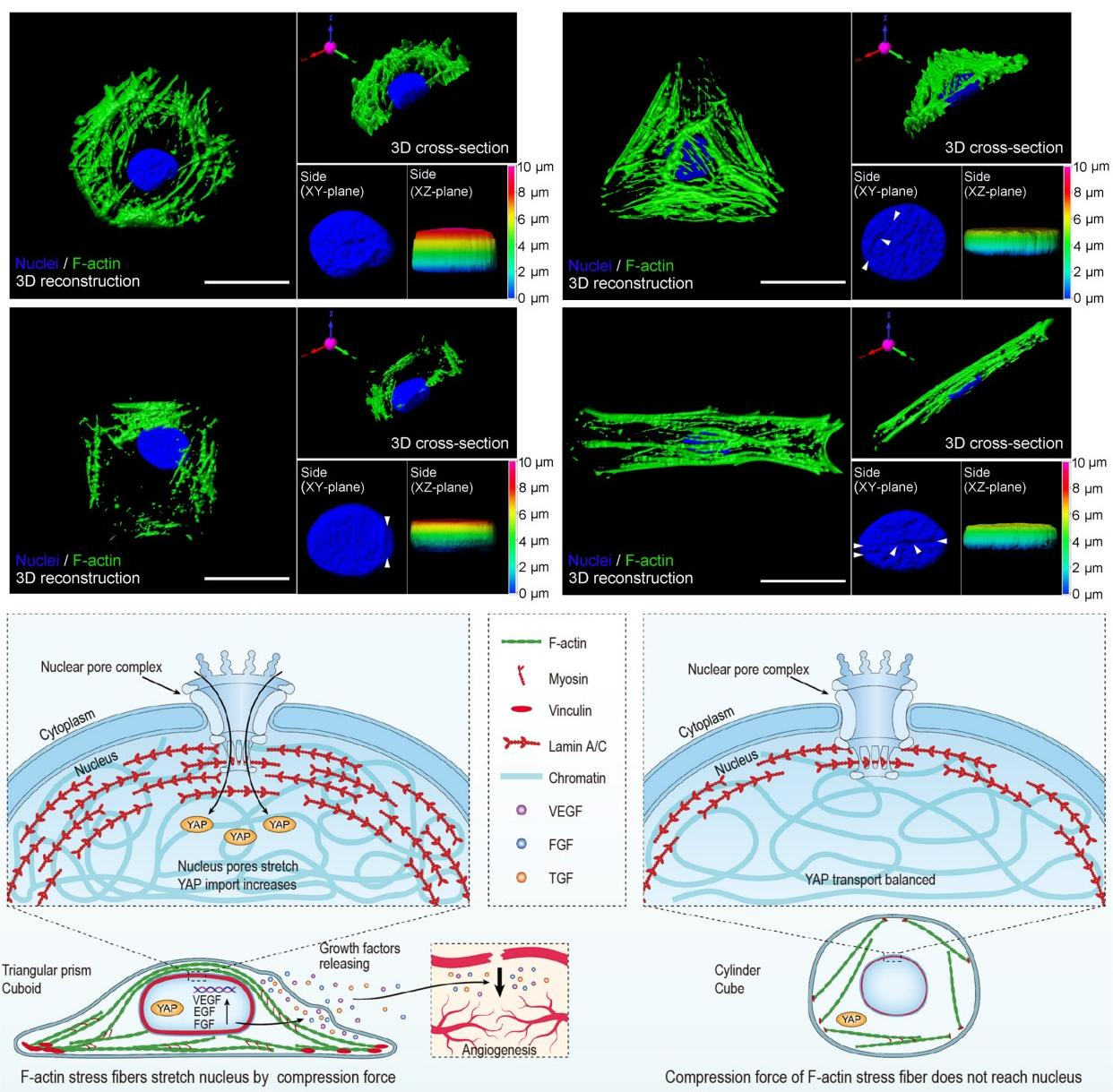
图2.3D微图案触发MSCs力学信号转导通路进而调控干细胞旁分泌功能
张胜民教授团队利用光刻微制造技术制备了具有不同3D几何形状的水凝胶微图案阵列,单细胞入孔率达75%以上。该研究提出了3D微图案力(3D Micropattern Force)的概念,并阐明了3D微图案调控人骨髓间充质干细胞力学信号转导的机制:3D微图案力通过调控细胞骨架空间重组,引起核孔拉伸变形,触发YAP入核,进一步通过力学信号转导途径调控干细胞旁分泌,从而促进血管化组织再生。实验证实,三棱柱和长方体微图案调控细胞中F-actin纤维的取向性增加并有序分布在细胞核上。细胞核受到压缩力,导致核孔被拉伸,降低了核孔对YAP入核的物理性屏障限制,从而促进YAP细胞核转运。上述微图案调控的力学信号转导显著增强了细胞的旁分泌功能,血管内皮生长因子、成纤维细胞生长因子和转化生长因子等基因表达和蛋白分泌水平上调,进而促进了体内血管生成和缺损部位皮肤组织再生。
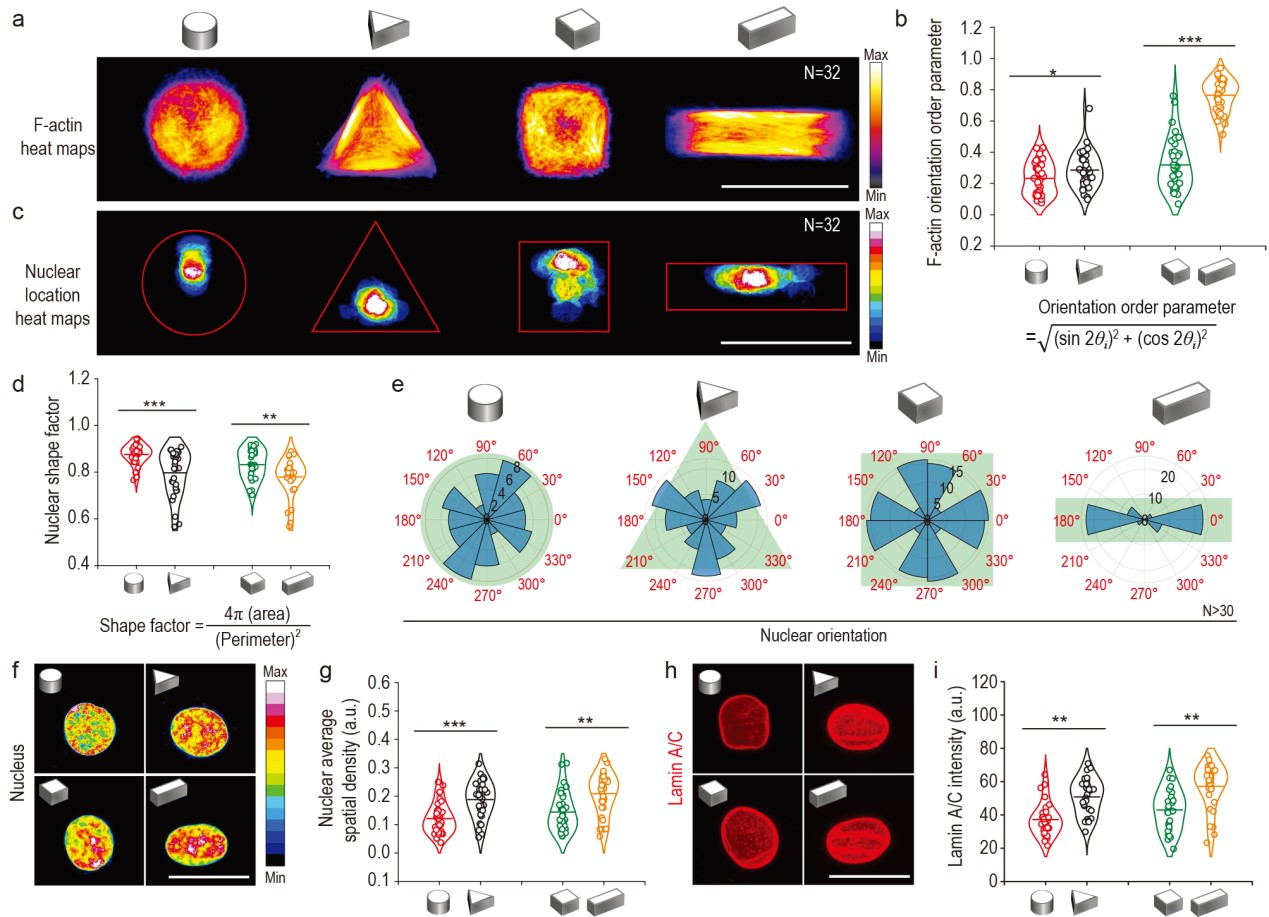
图3.3D微图案调控MSCs细胞核重塑和机械力
该工作克服了传统2D微图案无法模拟细胞天然3D微环境的限制,展示了特定形状的3D微图案在调控干细胞功能和组织再生方面的重要潜能,并将为新一代细胞/基因活性生物材料的创新设计提供重要理论依据。11月6日,《中国科学》杂志社对该工作进行了报道。
华中科技大学生命学院博士生李艳和钟振宇为论文共同第一作者,张胜民教授和杜莹莹副教授为共同通讯作者。该研究得到了国家自然科学基金重点项目(31430029)、中国科协青年人才托举工程(YESS20200077)等项目的支持。
《国家科学评论》论文原文链接:https://doi.org/10.1093/nsr/nwad165
《国家科学评论》亮点点评链接:https://doi.org/10.1093/nsr/nwad198
(来源:华中科技大学新闻网)



 微信公众号
微信公众号
 下载app
下载app
 京公网安备 11010202008974号
京公网安备 11010202008974号